גידולי מוח הם מצב שבו תאים במוח או ברקמות הסמוכות לו מתחילים להתחלק באופן בלתי מבוקר וליצור מסה של תאים. גידולים אלו יכולים להיות שפירים (לא סרטניים) או ממאירים (סרטניים).
המשמעות הקלינית של גידול מוח אינה נקבעת רק על פי סיווגו כשפיר או ממאיר. אלא בעיקר לפי מיקומו, גודלו, קצב הגדילה שלו וההשפעה שלו על מבנים סמוכים. בהתאם למיקום, גם גידול קטן יחסית עלול לגרום לפגיעה תפקודית משמעותית. למשל בתנועה, דיבור, ראייה או תפקודים קוגניטיביים. בעוד שגידולים הגדלים באיטיות וללא תגובה סביבתית משמעותית (כגון בצקת), עשויים להגיע לממדים גדולים טרם הופעת תסמינים.
בשנים האחרונות חלה התקדמות משמעותית בתחום, הכוללת הדמיה מתקדמת ומיפוי מוחי תפקודי. כמו כן, קיימים טכניקות ניתוח מיקרוכירורגיות ושילוב טיפולים משלימים. אלו מאפשרים כיום טיפול מדויק ומותאם אישית, תוך שמירה מרבית על תפקוד ואיכות חיים.
גידולי מוח שפירים הם גידולים שאינם סרטניים ואינם שולחים גרורות. אך בשל מיקומם בתוך הגולגולת הם עלולים לגרום לתסמינים משמעותיים. למרות קצב גדילה איטי יחסית, גם גידול שפיר יכול להשפיע על תפקוד המוח באמצעות לחץ על רקמת מוח, עצבים קרניאליים או מבנים סמוכים.
גידולים שפירים מתפתחים לרוב מרקמות תומכות ולא מתאי עצב עצמם. הם כוללים בין היתר:
לכל אחד מהגידולים הללו יש מאפיינים שונים מבחינת המיקום במוח, גיל ההופעה, קצב הגדילה והטיפול הנדרש.
התסמינים של גידולי מוח שפירים משתנים בהתאם למספר גורמים:
במקרים רבים הגידול גדל באיטיות ולכן התסמינים מתפתחים בהדרגה.
התסמינים האפשריים יכולים לכלול:
לעיתים, במיוחד כאשר מדובר בגידולים קטנים, אין כלל תסמינים, והגידול מתגלה במקרה במהלך בדיקות הדמיה.
האבחון של גידולי מוח שפירים מתבצע באמצעות שילוב של הערכה קלינית ובדיקות הדמיה מתקדמות. הן מאפשרות לזהות את מיקום הגידול, מאפייניו והשפעתו על מבני המוח הסמוכים. הבדיקות המרכזיות כוללות:
MRI מוח
זוהי הבדיקה המדויקת והחשובה ביותר לאבחון גידולי מוח. בדיקת הMRI מאפשרת להעריך את מיקומו המדויק של הגידול, גודלו ויחסו למבנים סמוכים. כמו כן, אנו יכולים לזהות מאפיינים נוספים כגון האדרה לאחר הזרקת חומר ניגוד (המעידה על פעילות הגידול) ונוכחות בצקת סביבו.
DTI (Diffusion Tensor Imaging)
מדובר ברצף מתקדם של MRI המדגים את מסילות החומר הלבן במוח. בדיקה זו מאפשרת מיפוי של מסלולים עצביים חשובים הקשורים לתפקודים כגון דיבור, ראייה ותנועה. הבדיקה מהווה כלי חשוב במיוחד בתכנון ניתוחים להסרת גידולים.
CT מוח
בדיקה זו משמשת לעיתים קרובות כבדיקה ראשונית. במיוחד במצבים דחופים. בדיקת ה CT מאפשרת לזהות קיומו של גידול תוך-גולגולתי. אם כי רגישותו נמוכה יותר בהדגמת רקמת המוח בהשוואה ל-MRI. יתרונו הוא בהדגמת מעורבות של עצם הגולגולת וכן בזיהוי הסתיידויות בתוך הגידול.
בהתאם לסוג הגידול ולמיקומו עשויות להתבצע גם:
במקרים מסוימים ניתן לאבחן את סוג הגידול על סמך ההדמיה בלבד. במקרים אחרים, האבחנה הסופית מתקבלת לאחר ניתוח להסרה או ביופסיה.
אפשרויות הטיפול בגידולי מוח שפירים מותאמות באופן אישי לכל מטופל, בהתאם לסוג הגידול, מיקומו, גודלו, קצב גדילתו והמצב הקליני. האפשרויות העיקריות כוללות:
מעקב הדמייתי כאשר מדובר בגידול קטן בעל מאפיינים שפירים שאינו גורם לתסמינים. ניתן לעיתים לבחור בגישה של מעקב בלבד. במקרים אלו מבוצעות בדיקות MRI תקופתיות לצורך הערכת יציבות הגידול, ללא צורך בהתערבות מיידית.
ניתוח להסרת הגידול (דרך קרניוטומיה, בגישה אנדוסקופית טרנס נזאלית, או דרך ארובת העין). במקרים רבים ניתן להסיר את הגידול באמצעות ניתוח נוירוכירורגי. בחירת הגישה הניתוחית נקבעת בהתאם למיקום הגידול, גודלו, יחסו למבנים סמוכים ומאפייניו הביולוגיים. קיימות מגוון גישות החל מקרניוטומיה, גישה אנדוסקופית דרך האף, וגישות דרך ארובת העין. כאשר מתאפשרת הסרה מלאה, הניתוח עשוי להוות טיפול מרפא. תכנון הניתוח מתבסס על הדמיה מתקדמת ולעיתים גם על מיפוי מוחי תפקודי. מטרת הניתוח היא להשיג הסרה מקסימלית בטוחה של הגידול תוך שמירה מרבית על תפקוד נוירולוגי ואיכות החיים של המטופל.
טיפול קרינתי ממוקד במקרים מסוימים ניתן להשתמש בטכנולוגיות קרינה מתקדמות, כגון קרינה סטריאוטקטית, במטרה לעצור או להאט את גדילת הגידול. טיפול זה אינו כרוך בפתיחת הגולגולת, ומתאים במיוחד לגידולים קטנים, לגידולים הממוקמים באזורים עמוקים או רגישים. כמו כן, למטופלים אשר אינם מתאימים לניתוח בשל מחלות רקע או סיכון ניתוחי מוגבר.
מנינגיומות הן הגידולים השפירים השכיחים ביותר במוח, ומקורן בקרומי המוח. ברוב המקרים מדובר בגידולים עם מהלך איטי, אך מיקומם, עשוי להוביל לפגיעה תפקודית משמעותית.
סיווג (WHO)
מאפיינים מולקולריים
בשנים האחרונות זוהו תתי-סוגים מולקולריים של מנינגיומות:
סווג מנינגיומות מסייעים בהערכת:
טיפול
המטרה היא הסרה מלאה כאשר ניתן, תוך שמירה על תפקוד נוירולוגי.
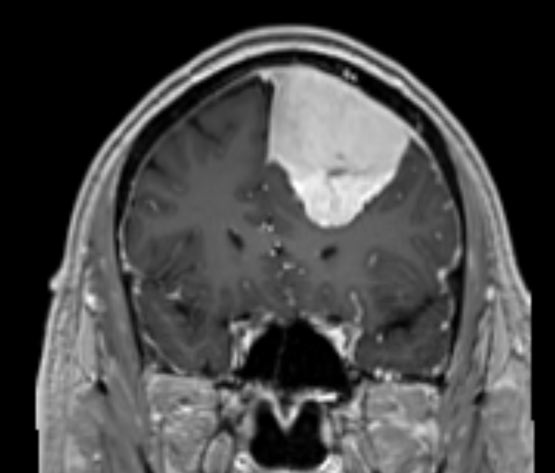
בת 60 עם שינויי התנהגות בשנה האחרונה, אובחנה עם מנינגיומה פארא סגיטלי אשר נותחה להסרה.
בלוטת ההיפופיזה היא בלוטה קטנה אך מרכזית, הממוקמת בבסיס המוח בתוך האוכף הטורקי, ומהווה את אחד הצמתים החשובים ביותר בוויסות המערכת ההורמונלית בגוף. דרך הפרשת הורמונים המפעילים בלוטות אחרות, ההיפופיזה שולטת בתהליכים חיוניים כגון גדילה, חילוף חומרים, תפקוד בלוטת התריס ויותרת הכליה, וכן בפוריות ובהנקה.
אדנומות של ההיפופיזה הן גידולים שפירים המתפתחים מתאי הבלוטה. למרות אופיים השפיר, המשמעות הקלינית שלהן עשויה להיות משמעותית, שכן הן עלולות להשפיע הן על המערכת ההורמונלית והן על מבנים אנטומיים סמוכים.
מקובל לחלק את האדנומות לשתי קבוצות עיקריות: אדנומות מתפקדות (functioning pituitary adenoma), המפרישות הורמונים באופן לא מבוקר, ואדנומות שאינן מתפקדות (non-functioning pituitary adenoma), אשר אינן מפרישות הורמונים באופן פעיל. אדנומות מתפקדות מתגלות לרוב בשלב מוקדם יחסית, עקב התסמונות ההורמונליות שהן גורמות. כך למשל, הפרשת יתר של הורמון הגדילה (GH) מובילה לאקרומגליה, הפרשת יתר של ACTH גורמת למחלת קושינג, והפרשת יתר של פרולקטין מובילה לפרולקטינומה שהיא הסוג השכיח ביותר. לעומת זאת, אדנומות שאינן מתפקדות עשויות להישאר אסימפטומטיות לאורך זמן, ולהתגלות רק כאשר הן גדלות וגורמות ללחץ על מבנים סמוכים.
הביטוי הקליני של אדנומות ההיפופיזה נובע אם כן משני מנגנונים עיקריים: הפרעה הורמונלית ו/או ואפקט מסה. הקרבה האנטומית של הבלוטה לעצבי הראייה ולכיאזמה האופטית גורמת להמיאנופסיה ביטמפורלית. לחץ על הרקמה התקינה של בלוטת ההיפופיזה עלול לגרום לחסר הורמונלי (היפופיטואיטריזם), ולעיתים גם לכאבי ראש.
בשנים האחרונות התפתח גם הסיווג המולקולרי והתאי של אדנומות ההיפופיזה, המבוסס על קווי התמיינות של תאי הבלוטה. סיווג זה כולל קבוצות כגון Pit-1, Tpit ו-SF-1, ומשקף את מקור התא ואת סוג ההורמון המופרש. לצד זאת, מדדים כמו Ki-67 מסייעים בהערכת קצב החלוקה של התאים והפוטנציאל האגרסיבי של הגידול. מידע זה תורם להבנה מדויקת יותר של התנהגות הגידול ולהתאמת המעקב והטיפול.
הטיפול באדנומות של ההיפופיזה מותאם באופן אישי לכל מטופל, ומשלב בין מספר גישות בהתאם לסוג הגידול ולביטויו הקליני. בפרולקטינומות, בנוסף לטיפול ניתוחי קיים טיפול תרופתי באמצעות אגוניסטים לדופמין המהווה לרוב קו טיפול ראשון ויכול להביא לירידה משמעותית בגודל הגידול ולנורמליזציה של רמות ההורמון. במרבית סוגי האדנומות האחרים, הטיפול המרכזי הוא ניתוח בגישה אנדוסקופית דרך האף (גישה טרנס-ספנואידלית), המאפשר גישה ישירה לאזור ההיפופיזה.
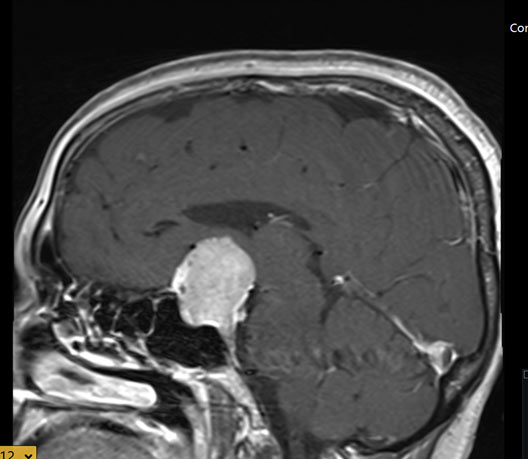
בן 45 עם מאקרואדנומה היפופיזרית, לא מפרישה אשר התגלתה בעיקבות הפרעת ראיה, אשר נותח להסרה בגישה אנדוסקופית טרנס ספנוידלית
גידולי מוח ממאירים הם גידולים סרטניים המתפתחים במוח (גידולים ראשוניים) או מגיעים אליו ממקומות אחרים בגוף (גידולים שניוניים). בניגוד לגידולים שפירים, גידולים ממאירים נוטים לגדול בקצב מהיר יותר. הם נוטים לחדור לרקמות מוח סמוכות ולהשפיע על תפקוד מערכת העצבים. נהוג לחלקם לשתי קבוצות עיקריות:
גידולים ראשוניים הם גידולים שמקורם בתאי המוח עצמו או בתאים הקשורים למערכת העצבים המרכזית. הם יכולים להתפתח מתאי עצב, מתאי התמיכה (גליה), מתאים המצפים את חדרי המוח (אפנדימה) או מתאים נוספים. בין הגידולים הראשוניים הממאירים ניתן למצוא:
גידולים אלו שונים מאוד זה מזה מבחינת ביולוגיה, קצב גדילה, דרכי טיפול ופרוגנוזה.
הסוג השכיח ביותר של גידולי מוח ראשוניים ממאירים. בשנים האחרונות חל שינוי מהותי בהבנת הגידולים הללו. הסיווג העדכני אינו מבוסס עוד רק על המראה ההיסטולוגי, אלא משלב גם מאפיינים מולקולריים וגנטיים, אשר קובעים את האבחנה, הפרוגנוזה והטיפול.
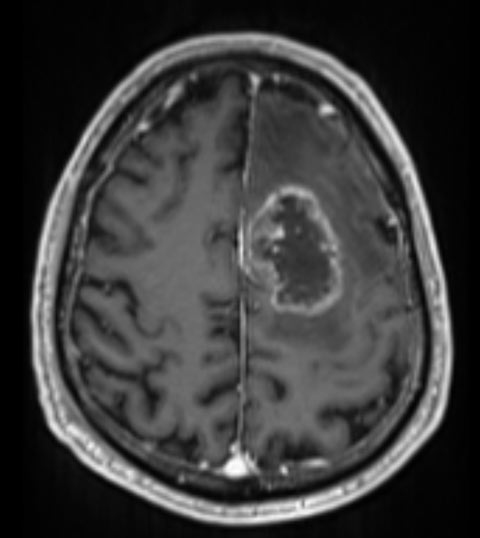
בן 65 עם גליומה מדרגה גבוהה באונה פרונטלית משמאל אשר נותח בעירות לכריתה.
IDH Mutation סמן פרוגנוסטי חשוב, קשור במהלך מחלה איטי יותר
MGMT promoter methylation מנבא תגובה טובה יותר ל Temozolomide
1p/19q codeletion אבחנתי לאוליגודנדרוגליומה, קשור לרגישות לטיפול ולשרידות ארוכה יותר
TERT, EGFR, CDKN2A/B deletion קשורים לאגרסיביות גבוהה
1. Astrocytoma, IDH-mutant
לרוב מופיע בגיל צעיר יותר.
• כולל דרגות 2–4
• גידול בדרגה 4 בקבוצה זו (עם מוטציה ב IDH) שונה ביולוגית מ Glioblastoma
• מוטציות אופייניות:
• IDH1/2
• ATRX loss
• TP53
• פרוגנוזה טובה יותר יחסית
2. Oligodendroglioma, IDH-mutant and 1p/19q-codeleted
• דורש שילוב של IDH mutation + 1p/19q codeletion לצורך אבחנה
• קיימות דרגות 2–3
• מאופיין ברגישות גבוהה לכימותרפיה וקרינה
• פרוגנוזה טובה יחסית
3. Glioblastoma, IDH-wildtype (WHO Grade 4)
• הגידול הממאיר והשכיח ביותר במבוגרים
• אבחנה יכולה להתבסס גם על סמנים מולקולריים, גם ללא מאפיינים היסטולוגים קלאסיים של Grade 4 (נמק, שגשוג כלי דם)
• מאפיינים מולקולריים אופיינים לגליובלסטומה:
TERT promoter mutation
EGFR amplification
+7/−10 chromosome signature
מהלך מחלה אגרסיבי
הקלסיפיקציה המולקולרית החדשה משנה באופן מהותי את אופן קבלת ההחלטות הטיפוליות בגליומות:
הטיפול בגליומות כיום מבוסס על שילוב של מספר מרכיבים:
1. ניתוח: המטרה היא הסרה מקסימלית בטוחה (Maximal Safe Resection) תוך שמירה על תפקוד נוירולוגי, תוך שימוש במיפוי מוחי.
2. קרינה ניתנת לאחר הניתוח, פועלת להשמדת תאים מיקרוסקופיים שנותרו, חשובה במיוחד בגידולים בדרגה גבוהה.
3. כימותרפיה: לרוב Temozolomide הניתנת בכדורים, לרוב בשילוב עם קרינה ולאחריה (פרוטוקול ( Stupp (יעילותו מושפעת מסטטוס MGMT methylation. הוא מהווה טיפול סטנדרטי בעיקר בGlioblastoma במקרים מסוימים (כגון אוליגודנדרוגליומה): נעשה שימוש גם בפרוטוקול PCV.
4. טיפולים ממוקדים- מעכבי IDH : בגליומות עם מוטציית IDH קיימים טיפולים במעכבים:
Vorasidenib (Voranigo) מעכב IDH1/2 פומי החודר למוח. היתרונות כוללים עיכוב התקדמות המחלה, דחיית קרינה וכימותרפיה (במיוחד בגידולים בדרגה נמוכה), טיפול מותאם לפרופיל הביולוגי של הגידול.
5. TTFields (Tumor Treating Fields: טיפול המבוסס על שדות חשמליים המעכבים חלוקת תאים סרטניים:
יתרונות:
גרורות מוחיות הן הגידולים הממאירים השכיחים ביותר במוח במבוגרים. מקורן בגידול ראשוני באיבר אחר, המתפשט למוח דרך מחזור הדם. מקורות שכיחים לגרורות מוחיות כוללים סרטן ריאות, סרטן שד, מלנומה, סרטן מעי גס וכליה. גרורות יכולות להופיע כמוקד בודד או כמספר גרורות במוח.
בשנים האחרונות חלה התקדמות משמעותית בהבנת הביולוגיה של גרורות מוחיות. עם מעבר לגישה המבוססת על מאפיינים מולקולריים של הגידול הראשוני:
הטיפול מותאם באופן אישי בהתאם למספר הגרורות, מיקומן, גודלן, מצב המחלה הסיסטמית, מוטציות ומצבו הכללי של המטופל:
הטיפול בגידולי מוח ממאירים עבר בשנים האחרונות שינוי משמעותי, עם מעבר לגישה מולקולרית-מותאמת אישית. שילוב בין טיפול מקומי (ניתוח וקרינה) לבין טיפול סיסטמי מתקדם מאפשר שליטה טובה יותר במחלה ושיפור באיכות החיים של המטופלים.